阿佛加德罗定律及几个导出关系式
来源:互联网发布时间:2009-07-29
阿佛加德罗定律认为:在同温同压下,相同体积的气体含有相同数目的分子。1811 年由意大利化学家阿佛加德罗提出假说,后来被科学界所承认。这一定律揭示了气体反应的体积关系,用以说明气体分子的组成,为气体密度法测定气态物质的分子量提供了依据。对于原子分子说的建立,也起了一定的积极作用。中学化学中,阿佛加德罗定律占有很重要的地位。它使用广泛,特别是在求算气态物质分子式、分子量时,如果使用得法,解决问题很方便。
下面简介几个根据克拉伯龙方程式导出的关系式,以便更好地理解和使用阿佛加德罗定律。克拉伯龙方程式通常用下式表示:PV=nRT……①P表示压强、V表示气体体积、n表示物质的量、T表示绝对温度、R表示气体常数。所有气体R值均相同。如果压强、温度和体积都采用国际单位(SI),R=8.31帕·米3/摩尔·度。如果压强为大气压,体积为升,则R=0.082大气压·升/摩尔·度。因为 n=M/M、 ρ=M/V(n—物质的量, M—物质的质量,M—物质的摩尔质量,数值上等于物质的分子量,ρ—气态物质的密度),所以克拉伯龙方程式也可写成以下两种形式:
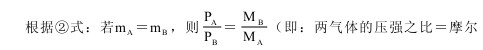
下面简介几个根据克拉伯龙方程式导出的关系式,以便更好地理解和使用阿佛加德罗定律。克拉伯龙方程式通常用下式表示:PV=nRT……①P表示压强、V表示气体体积、n表示物质的量、T表示绝对温度、R表示气体常数。所有气体R值均相同。如果压强、温度和体积都采用国际单位(SI),R=8.31帕·米3/摩尔·度。如果压强为大气压,体积为升,则R=0.082大气压·升/摩尔·度。因为 n=M/M、 ρ=M/V(n—物质的量, M—物质的质量,M—物质的摩尔质量,数值上等于物质的分子量,ρ—气态物质的密度),所以克拉伯龙方程式也可写成以下两种形式: